放生研の研究成果を一般の方にわかりやすく紹介する研究成果アーカイブです。
2016年以前のアーカイブはこちらです。
膵臓がん内部に低酸素で間質に富む微小環境が形成される原因を特定!(2018年1月)
| 膵臓がんは繊維芽細胞やコラーゲン繊維などの間質成分および低酸素領域に富み、これが抗がん剤や放射線治療への抵抗性を引き起こしていると考えられています。がん細胞生物学分野では、低酸素がん細胞内部で活性化した低酸素低酸素誘導性因子1(hypoxia-inducible factor1:HIF-1)が、ソニックヘッジホッグ蛋白質の産生と分泌を促し、これががん関連繊維芽細胞の増殖を促して、膵臓がんに特徴的な微小環境の形成を担っていることを解明しました。そしてがん治療に於いてがん細胞と癌関連繊維芽細胞の相互作用を遮断する意義を示しました。(https://www.ncbi.nlm.nih.gov/pubmed/29535824) |
|
がん細胞の低酸素応答と悪性化で機能するHIF-1の新規活性化機構の解明!(2017年11月)
| 低酸素誘導性転写因子1(hypoxia-inducible factor1:HIF-1)はがん細胞の悪性化を導く遺伝子であり、その活性化機構を解明することが急務である。がん細胞生物学分野では、Period 2(PER2)という遺伝子が、HIF-1とDNAの結合を促進する新しいタイプのHIF-1活性化因子であることを発見しました。PER2は周期性をもって活性化する遺伝子であることから、がんの悪性度に日内周期がある可能性が示唆されました。(https://www.ncbi.nlm.nih.gov/pubmed/28963769)。 |
|
がん細胞が放射線治療抵抗性を獲得するメカニズムの解明!(2017年7月)
| 放射線治療はがん治療における三本柱の一つで、近年の高精度化には目を見張るものがあります。しかし、これまでの基礎研究および臨床研究から「がん細胞が低酸素誘導性因子1(hypoxia-inducible factor1:HIF-1)という遺伝子を用いて放射線治療を生き延びている可能性」が指摘され、HIF-1が機能するメカニズムの解明が求められていました。がん細胞生物学分野では、HIF-1を活性化する新規遺伝子としてUbiquitin C-terminal hydrolase-L1(UCHL1)を同定し、UCHL1がHIF-1を活性化することによってがん細胞の放射線抵抗性が亢進することを証明しました。また、UCHL1-HIF-1経路を遮断することによって、放射線治療の効果を向上させられることを示し、新たな治療法の確立に向けた道を拓きました。(https://www.ncbi.nlm.nih.gov/pubmed/28761052)。 |
|
小児血液疾患で白血病を引き起こすファンコニ貧血の原因遺伝子を発見!(2017年7月)
| ファンコニ貧血はまれな小児の遺伝性疾患で、白血病やがん、再生不良性貧血などを引き起こす重篤な難病です。その原因は、自然に発生するゲノムの傷をなおすための細胞内のメカニズムが働かなくなっているためで、アンジェリーナジョリー氏で有名になった家族性乳がんとも関係の深い病気です。いままでに21種類の原因遺伝子が報告されていましたが、今回、放射線生物研究センターの研究者は、ドイツのビュルツブルグ大学と共同研究し、あらたに22番目のファンコニ貧血の原因となる遺伝子を見つけ出しました。これは、細胞内でゲノムの傷を修復するナノマシンの22個目の部品を見つけたことにあたります。発がんの予防や、再生不良性貧血の治療などを考えるうえで大事な発見で、米国の一流科学雑誌Mol Cell誌とJCI誌に発表されました。ライフサイエンス新着論文レビューで詳しく解説しています(http://first.lifesciencedb.jp/archives/16605)。 |
 |
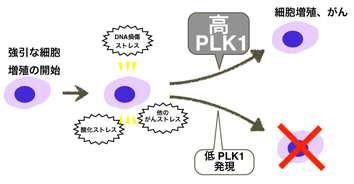
がん細胞のゲノムDNA損傷を乗り越えて増殖する仕組み(2017年12月)
| がん細胞がゲノムDNA損傷などの障害を乗り越えて増殖することができます。遺伝情報がコードされているゲノムDNAが傷つきながらも増殖することができる、このがん細胞特有の性質を作り上げるためのシグナル伝達経路を私たちは同定しました。CDKとPLK1という二つのリン酸化酵素が関わっており、細胞分裂を促進させると同時に、細胞の中に生じたゲノムDNA損傷の検出機構を働かなくさせるといった二通りの方法で細胞増殖を推し進める経路でした。この新規のリン酸化シグナル経路はある種のがん細胞では強く働いており、今後の治療を考える上で重要な知見となります。本研究の成果はeLIFE誌に公開されました。(https://elifesciences.org/articles/29953) |
 |


